1.5.2.8. Иммунная система
| Листать назад | Оглавление | Листать вперед |
Как наш организм защищается от инфекции. Иммунитет – естественная защита от инфекций, виды иммунитета. Иммунная система
Еще в древнем Египте и Греции за больными чумой ухаживали люди, прежде переболевшие этой болезнью: опыт показывал, что они уже не подвержены заражению.
Люди интуитивно пытались обезопасить себя от инфекционных болезней. Несколько веков назад в Турции, на Ближнем Востоке, в Китае для профилактики оспы втирали в кожу и слизистые оболочки носа гной из подсохших оспенных гнойников. Люди надеялись, что, переболев каким-то инфекционным заболеванием в легкой форме, они приобретут устойчивость к действию возбудителей в последующем.
Так зарождалась иммунология – наука, изучающая реакции организма на нарушение постоянства его внутренней среды.
Нормальное состояние внутренней среды организма является залогом правильного функционирования клеток, не общающихся напрямую с внешним миром. А такие клетки образуют большинство наших внутренних органов. Внутреннюю среду составляют межклеточная (тканевая) жидкость, кровь и лимфа, а их состав и свойства во многом контролирует иммунная система .
Трудно найти человека, который не слышал бы слово “иммунитет”. Что же это такое?
 |  |
Другими словами, это невосприимчивость организма к инфекционным агентам и веществам, обладающим антигенными свойствами.
Антигены – общее название чужеродных для организма агентов и веществ. Ими могут быть продукты жизнедеятельности микроорганизмов – возбудителей различных заболеваний, ядовитые соединения растительного и животного происхождения, погибшие или переродившиеся клетки самого организма и другие вещества.
В жизни нас окружает бесчисленное множество невидимых простым глазом микроорганизмов, многие из которых очень опасны для организма. Поражает их воспроизводство. Одна бактерия в течение 1 ч порождает 8 себе подобных особей, через 2 ч их образуется уже 64, через 24 ч – 4772 триллиона. При размножении в течение 1 года получилась бы масса бактерий, равная массе Солнца. Но в природе все находится в равновесии и беспрепятственного увеличения числа микробов не происходит. Научился сопротивляться этим агрессорам и наш организм.
В нашем организме есть особые механизмы, препятствующие проникновению в него микробов и развитию инфекций. Так, слизистые оболочки выполняют роль барьера, через который проходят далеко не все микробы, а выделяемые кожным эпителием и слизистыми оболочками вещества понижают активность микробов или полностью их инактивируют. Одним из главных механизмов сопротивления является иммунная система.
Строение и состав иммунной системы. Иммунная система человека (рисунок 1.5.13) включает центральные органы – костный мозг и вилочковую железу (тимус) – и периферические – селезенку, лимфатические узлы, лимфоидную ткань. Эти органы вырабатывают несколько типов клеток, которые и осуществляют надзор за постоянством клеточного и антигенного состава внутренней среды.

Рисунок 1.5.13. Основные органы иммунной системы человека
Основные клетки иммунной системы – фагоциты и лимфоциты (В- и Т-лимфоциты). Они циркулируют по кровеносной и лимфатической системе, некоторые из них могут проникать в ткани. Все клетки иммунной системы имеют определенные функции и работают в сложном взаимодействии, которое обеспечивается выработкой специальных биологически активных веществ – цитокинов . Вы, наверное, слышали такие названия, как интерфероны , интерлейкины и тому подобные. Это так называемые цитокины, с помощью которых клетки иммунной системы могут обмениваться информацией и осуществлять координацию своих действий.
Фагоциты (в переводе на русский язык – “пожирающие”) бросаются на пришельцев, поглощая и разрушая микробы, ядовитые вещества и другие чужеродные для организма клетки и ткани. При этом погибают и сами фагоциты, высвобождая вещества ( медиаторы ), вызывающие местную воспалительную реакцию и привлекающие новые группы фагоцитов на борьбу с антигенами.
Впервые фагоциты – “подвижные клетки” открыл в 1882 году И.И. Мечников, когда проводил опыт, вводя в тело личинок морских звезд шип от розы. Он увидел, как занозу быстро окружают клетки и пытаются ее уничтожить.
Этот процесс был назван И.И. Мечниковым фагоцитозом , а клетки, осуществляющие эту функцию, – фагоцитами . Установлено, что один фагоцит может захватить 15-20 бактерий. Если он поглощает больше микробов, чем может их переварить, то клетка гибнет. Смесь погибших и живых фагоцитов и бактерий называется гноем.
Известно, что при многих заболеваниях повышается температура, возникает воспалительный процесс.
 |  |
Лимфоциты вырабатывают специфические белки ( антитела ) – иммуноглобулины , взаимодействующие с определенными антигенами и связывающие их. Антитела нейтрализуют активность ядов, микробов, делают их более доступными для фагоцитов.
 |  |
Иммунная система “запоминает” те чужеродные вещества, с которыми она хоть раз встречалась и на которые реагировала. От этого зависит формирование невосприимчивости к “чужим” агентам, терпимости к собственным биологически активным веществам и повышенной чувствительности к аллергенам. Нормально функционирующая иммунная система не реагирует на внутренние факторы и, в то же время, отторгает чужеродные воздействия на организм. Она формирует иммунитет – противоинфекционный, трансплантационный, противоопухолевый. Иммунитет защищает организм от инфекционных болезней, освобождает его от погибших, переродившихся и ставших чужеродными клеток. Иммунные реакции являются причиной отторжения пересаженных органов и тканей. При врожденных или приобретенных дефектах иммунной системы возникают заболевания – иммунодефицитные, аутоиммунные или аллергические, вызванные повышенной чувствительностью организма к аллергенам .
Виды иммунитета . Различают естественный и искусственный иммунитет (смотри рисунок 1.5.14).

Рисунок 1.5.14. Виды иммунитета
Человек уже с рождения невосприимчив ко многим болезням. Такой иммунитет называют врожденным . Например, люди не болеют чумой животных, потому что у них в крови уже содержатся готовые антитела. Врожденный иммунитет передается по наследству от родителей. Организм получает антитела от матери через плаценту или с материнским молоком. Поэтому часто у детей, находящихся на искусственном вскармливании, ослаблен иммунитет. Они больше подвержены инфекционным заболеваниям и чаще страдают от диабета. Врожденный иммунитет сохраняется всю жизнь, но он может быть преодолен, если дозы заражающего агента увеличатся или ослабеют защитные функции организма.
В некоторых случаях иммунитет возникает после перенесенных заболеваний. Это приобретенный иммунитет . Переболев один раз, люди приобретают невосприимчивость к возбудителю. Такой иммунитет может сохраняться десятки лет. Например, после кори остается пожизненный иммунитет. Но при других инфекциях, например при гриппе, ангине, иммунитет сохраняется относительно недолго, и человек может перенести эти заболевания несколько раз в течение жизни. Врожденный и приобретенный иммунитет называют естественным.
Инфекционный иммунитет всегда конкретен или, другими словами, специфичен. Он направлен только против определенного возбудителя и не распространяется на прочих.
Существует также искусственный иммунитет, который возникает в результате введения в организм готовых антител. Это происходит, когда заболевшему человеку вводят сыворотку крови переболевших людей или животных, а также при введении ослабленных микробов – вакцины . В этом случае организм активно участвует в выработке собственных антител, и такой иммунитет остается на длительное время. Об этом подробнее будет сказано в главе 3.10.
Как устроен иммунитет: Объясняем по пунктам
Андрей Смирнов СПИД.ЦЕНТР
«Йогурт для укрепления иммунитета», «Иммуностимулирующие витамины», «Да простудился, наверное, иммунитет упал»… Мы слышим слово «иммунитет» так часто, что уже почти не задумываемся, как он устроен и работает. На уроках биологии нам рассказывали, что иммунитет защищает от микробов, но только ли этим ограничивается его функция и как именно он понимает, от кого нужно нас защищать? СПИД.ЦЕНТР объясняет, как устроена иммунная система.
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
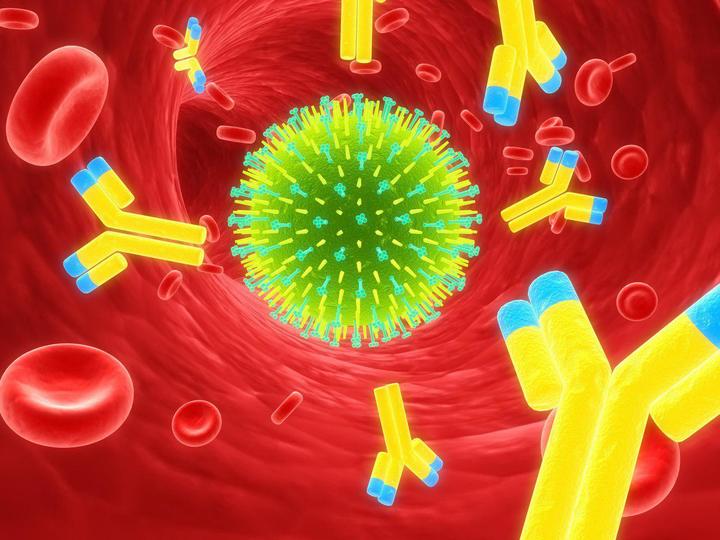
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
по теме

Мнение
«Иммунитет пациента с ВИЧ похож на иммунитет пожилого человека»
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
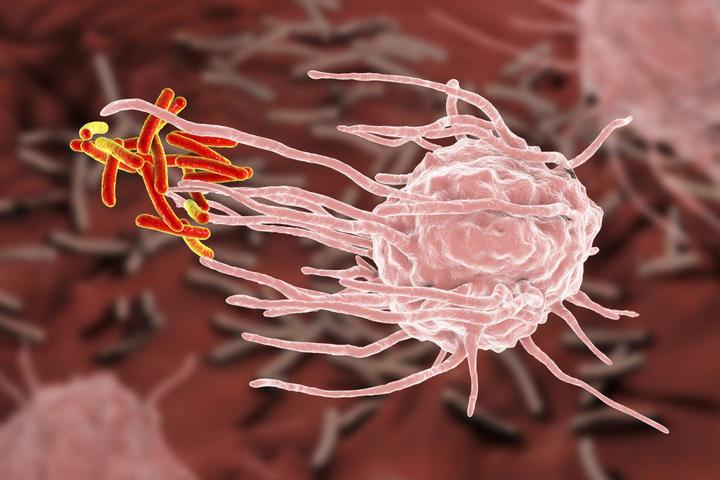
Кто отвечает за работу различных видов иммунитета?
- Костный мозг. Это центральный орган иммуногенеза. В костном мозге образуются все клетки, участвующие в иммунных реакциях.
- Тимус (вилочковая железа). В тимусе происходит дозревание некоторых иммунных клеток (Т-лимфоцитов) после того, как они образовались в костном мозге.
- Селезенка. В селезенке также дозревают иммунные клетки (B-лимфоциты), кроме того, в ней активно происходит процесс фагоцитоза — когда специальные клетки иммунной системы ловят и переваривают проникших в организм микробов, фрагменты собственных погибших клеток и так далее.
- Лимфатические узлы. По своему строению они напоминают губку, через которую постоянно фильтруется лимфа. В порах этой губки есть очень много иммунных клеток, которые также ловят и переваривают микробов, проникших в организм. Кроме того, в лимфатических узлах находятся клетки памяти — это специальные клетки иммунной системы, которые хранят информацию о микробах, уже проникавших в организм ранее.
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
- Т-лимфоциты. Названы так, потому что после образования в костном мозге дозревают в вилочковой железе — тимусе. Разные подвиды Т-лимфоцитов отвечают за разные функции. Например, Т-киллеры могут убивать зараженные вирусами клетки, чтобы остановить развитие инфекции, Т-хелперы помогают иммунной системе распознавать конкретные виды микробов, а Т-супрессоры регулируют силу и продолжительность иммунной реакции.
- B-лимфоциты. Название их происходит от Bursa fabricii (сумка Фабрициуса) — особого органа у птиц, в котором впервые обнаружили эти клетки. В-лимфоциты умеют синтезировать антитела (иммуноглобулины). Это специальные белки, которые «прилипают» к микробам и вызывают их гибель. Также антитела могут нейтрализовывать некоторые токсины.
- Натуральные киллеры. Эти клетки находят и убивают раковые клетки и клетки, пораженные вирусами.
- Нейтрофилы и макрофаги умеют ловить и переваривать микробов — осуществлять фагоцитоз. Кроме того, макрофаги выполняют важнейшую роль в процессе презентации антигена, когда макрофаг знакомит другие клетки иммунной системы с кусочками переваренного микроба, что позволяет организму лучше бороться с инфекцией.
- Эозинофилы защищают наш организм от паразитов — обеспечивают антигельминтный иммунитет.
- Базофилы — выполняют главным образом сигнальную функцию, выделяя большое количество сигнальных веществ (цитокинов) и привлекая этим другие иммунные клетки в очаг воспаления.

Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
по теме
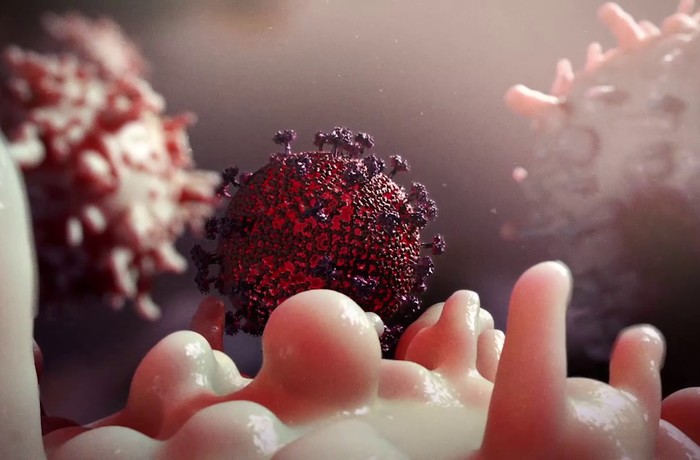
Эпидемия
Учёные выяснили, как вирусы обманывают иммунитет
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
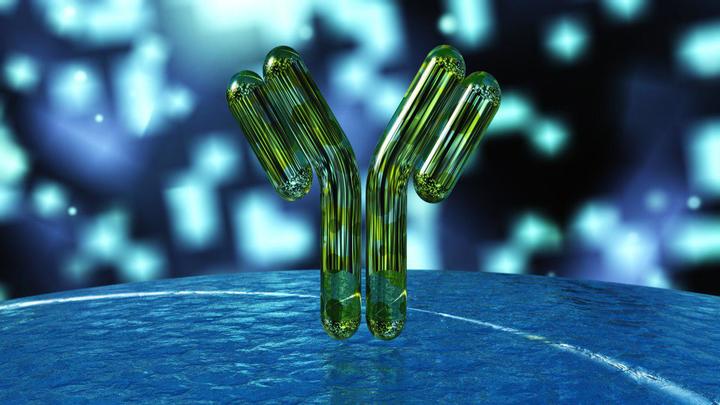
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
Иммунитет человека
 Пожалуй, каждый знает, насколько важным является иммунитет человека. Но далеко не все представляют, что означает это понятие. В основном оно ассоциируется у людей с защитой организма, что не совсем верно. Иммунитет человека – это способность организма сопротивляться различным болезнетворным влияниям, в частности инфекционным агентам и вредным бактериям. Благодаря иммунной системе, постоянно поддерживается состояние невосприимчивости к определенным микроорганизмам, а также к их продуктам жизнедеятельности. Компоненты иммунной системы распознают и разрушают чужеродные структуры (антигены), которые попадают из внешней среды или становятся опасными изнутри. Реакция иммунной системы организма на внедрение вирусов, грибов, паразитов, как правило, незамедлительная. Как только микроб попадает в организм, к нему устремляются иммунные клетки.
Пожалуй, каждый знает, насколько важным является иммунитет человека. Но далеко не все представляют, что означает это понятие. В основном оно ассоциируется у людей с защитой организма, что не совсем верно. Иммунитет человека – это способность организма сопротивляться различным болезнетворным влияниям, в частности инфекционным агентам и вредным бактериям. Благодаря иммунной системе, постоянно поддерживается состояние невосприимчивости к определенным микроорганизмам, а также к их продуктам жизнедеятельности. Компоненты иммунной системы распознают и разрушают чужеродные структуры (антигены), которые попадают из внешней среды или становятся опасными изнутри. Реакция иммунной системы организма на внедрение вирусов, грибов, паразитов, как правило, незамедлительная. Как только микроб попадает в организм, к нему устремляются иммунные клетки.
Общая сопротивляемость организма
В результате вокруг микроорганизма формируется очаг воспаления, который с одной стороны является барьером, направленным на предотвращение распространения возбудителя, а с другой – предупреждает организм о вторжении чужеродного агента. Далее происходит распознавание опасного агента и выработка факторов защиты против конкретного микроба, а также его частичное разрушение. Кроме того, формируется иммунологическая память о данных процессах, благодаря которой при следующей атаке этого микроба (антигена) запуститься сигнал для распознавания его особыми клетками иммунной системы. После того, как микроб изолирован и распознан, он подвергается полному уничтожению.
Клеточный и гуморальный иммунитет
Все защитные реакции в организме осуществляются за счет разных компонентов иммунитета: клеток и белков. Макрофаги и некоторые лимфоциты формируют клеточное звено. Причем макрофаги захватывают и переваривают чужеродные структуры, а затем передают информацию об этом лимфоцитам. В клеточном звене образуется клон лимфоцитов (разновидность белых клеток крови), который обладает способностью разрушать мембраны, так называемых клеток-мишеней, где имеются чужеродные структуры. Гуморальный иммунитет человека обеспечивается специфическими белками (антителами). Его действие реализуется через В-лимфоциты, которые еще не контактировали с антигенами, но после контакта они начинают активно вырабатываться антитела (иммуноглобулины, Ig), которые действуют на чужеродный агент. Эти белки обладают свойством прилипать к некоторым компонентам микроба, приводя к его разрушению или быстрому выведению из организма. Есть несколько видов антител, и каждый выполняет свою специфическую функцию.
Роль иммуноглобулинов
Антитела делятся на несколько классов: иммуноглобулины А, E, D, G, M. Иммуноглобулины типа А участвуют в первичном поверхностном контакте с микробами, в частности препятствуют проникновению микробов в организм, формируют антитоксический иммунитет. Они способны создавать особые полимерные формы – секреторный иммуноглобулин А. Именно этот иммуноглобулин препятствует прикреплению чужеродного агента к клеткам пограничных тканей (слизистых оболочек). Благодаря иммуноглобулинам типа G и M осуществляется защита организма от уже проникших внутрь инфекционных агентов. Ранними защитными белками являются иммуноглобулины М, а иммуноглобулины класса G являясь основным фактором гуморального звена иммунитета человека, отвечают за выздоровление организма в целом. К тому же, иммуноглобулины этого класса могут на протяжении долгого времени защищать от повторного внедрения различных микроорганизмов. Иммуноглобулины Е несут ответственность за возникновение аллергической реакции.
Функции интерферонов
В ответ на действие различных антигенов (к примеру, вирусов) клетки иммунной системы образуют сложные белковые соединения – интерфероны, которые осуществляют ряд защитный функций. Выделяют несколько типов интерферонов. Стоит отметить интерфероны 1 типа – альфа, которые обладают противовирусным эффектом. Человек, после инфицирования вирусным агентом некоторое время еще не знает о болезни (продромальный период инфекции). Но интерфероны альфа уже проявляют заботу. Они способны создавать невосприимчивость клеток к инфицированию вирусами, а в уже поврежденных клетках – блокируют размножение вирусов.
Механизм действия альфа-интерферонов
 Вирусы покрыты оболочкой, защищающей располагающиеся внутриядерные молекулы ДНК или РНК. Когда они проникают в клетку, оболочка разрушается и происходит производство вирусных белков. Формируется вирусное потомство – иногда миллионы новых копий вируса. Воспроизведенные таким образом вирусы ищут новые клетки. А пораженные клетки человека, как правило, погибают. Альфа-интерфероны устремляются к клетке с вирусом, запуская ряд сигнальных реакций и не дают вирусу возможности синтезировать собственные белки для начала размножения. Кроме того, альфа-интерфероны вступают в контакт с соседними клетками, изменяют свойства их мембран таким образом, что они становятся невосприимчивыми к атакам вирусов. К тому же, интерфероны 1 типа корректируют и восстанавливают иммунитет, а также помогают иммунной системе бороться с антигенами. Иммуномодулирующий эффект альфа-интерферонов заключается в том, они регулируют экспрессию белков HLA, участников формирования иммунного ответа, и чувствительность к информационным белковым молекулам (цитокинам), определяющих выживаемость иммунных клеток. Они также повышают активность естественных киллеров, которые устанавливают с пораженной клеткой прямой контакт и уничтожают ее. Помимо этого интерфероны усиливают действие макрофагов, которые захватывают чужеродные частицы и переваривают их. Интерфероны 1 типа увеличивают и стимулируют рост иммунных клеток, усиливая борьбу иммунной системы против возбудителей самых разных заболеваний.
Вирусы покрыты оболочкой, защищающей располагающиеся внутриядерные молекулы ДНК или РНК. Когда они проникают в клетку, оболочка разрушается и происходит производство вирусных белков. Формируется вирусное потомство – иногда миллионы новых копий вируса. Воспроизведенные таким образом вирусы ищут новые клетки. А пораженные клетки человека, как правило, погибают. Альфа-интерфероны устремляются к клетке с вирусом, запуская ряд сигнальных реакций и не дают вирусу возможности синтезировать собственные белки для начала размножения. Кроме того, альфа-интерфероны вступают в контакт с соседними клетками, изменяют свойства их мембран таким образом, что они становятся невосприимчивыми к атакам вирусов. К тому же, интерфероны 1 типа корректируют и восстанавливают иммунитет, а также помогают иммунной системе бороться с антигенами. Иммуномодулирующий эффект альфа-интерферонов заключается в том, они регулируют экспрессию белков HLA, участников формирования иммунного ответа, и чувствительность к информационным белковым молекулам (цитокинам), определяющих выживаемость иммунных клеток. Они также повышают активность естественных киллеров, которые устанавливают с пораженной клеткой прямой контакт и уничтожают ее. Помимо этого интерфероны усиливают действие макрофагов, которые захватывают чужеродные частицы и переваривают их. Интерфероны 1 типа увеличивают и стимулируют рост иммунных клеток, усиливая борьбу иммунной системы против возбудителей самых разных заболеваний.
По материалам:
“Иммунология в клинической практике”, К.А. Лебедев, И.Д.Понякина.
“Вторичные иммунодефициты: необходимость корректной диагностики и адекватной интерфероно- и иммунотерапии”, И.В. Нестерова.
Материалы подготовлены сотрудниками компании ООО «Ферон» на основе открытых информационных источников
Антитела IgG и IgM и клеточный иммунитет к COVID-19
” data-image-caption=”” data-medium-file=”https://unclinic.ru/wp-content/uploads/2021/09/antitela-igg-i-igm-i-kletochnyj-immunitet-k-covid-19-900×600.jpg” data-large-file=”https://unclinic.ru/wp-content/uploads/2021/09/antitela-igg-i-igm-i-kletochnyj-immunitet-k-covid-19.jpg” title=”Антитела IgG и IgM и клеточный иммунитет к COVID-19″>
Александр Попандопуло, студент медицинского института УЛГУ. Редактор А. Герасимова
- Запись опубликована: 24.09.2021
- Время чтения: 1 mins read
После прививок от COVID-19 многие пациенты сдают анализ на антитела, вырабатываемые в организме под воздействием вакцины. Тем не менее вакцина также стимулирует другой тип иммунитета, называемый клеточным.
Разберемся что такое клеточный и гуморальный иммунитет? Как проверить уровень антител? Означает ли отсутствие антител отсутствие иммунитета?
Что такое антитела к COVID-19?
Антитело (иммуноглобулин) – это белок, продуцируемый В-лимфоцитами и плазматическими клетками, стимулированными антигеном, то есть в случае заболевания COVID-19 – белком SARS-CoV-2 (в основном шиповым белком). Антитела создаются для нейтрализации патогенов, против которых они были произведены.
Антитела могут образовываться после контакта с возбудителем (вирусом или бактерией) или в результате введения вакцины против заболевания. Имеющиеся в настоящее время вакцины против COVID-19 стимулируют выработку в организме пайкового белка – антигена, стимулирующего выработку антител и иммунных клеток.
Антитела состоят из четырех пептидных цепей – двух легких и двух тяжелых, соединенных между собой специальными связями. Антитела в организме можно разделить на несколько классов: IgA, IgM, IgG, IgE, IgD. Принадлежность к классу зависит от структуры тяжелой цепи антитела.
Виды антител к COVID-19
В настоящее время серология фокусируется в первую очередь на определении антител классов IgG и IgM, направленных против SARS-CoV-2, хотя определяются и антитела класса IgA. Наиболее важные антитела к SARS-CoV-2 образуются в ответ на антигены – спайк-белок (S) и нуклеокапсидный белок вируса SARS-CoV-2.
- Спайк-белок располагается на поверхности вируса и образует его корону. Этот же белок позволяет вирусу проникать в клетки организма.
- Нуклеокапсидный белок (N) участвует, среди прочего, в репликации (дупликации) генетического материала вируса.
Примерно у 90% больных, перенесших инфекцию, вырабатываются антитела. Но можно заболеть COVID-19 и не иметь антител.
Как работают антитела класса IgG?
Антитела класса IgG обладают высоким сродством к антигену (и, следовательно, к патогену), и более того, они близки к антигену таким образом, что он доступен питающимся клеткам, которые его разрушают (фагоцитоз). Этот класс антител играет важную роль в иммунном ответе против микробов после защитной вакцинации.
Нужно ли носить маску
” data-image-caption=”” data-medium-file=”https://unclinic.ru/wp-content/uploads/2021/09/nuzhno-li-nosit-masku-900×600.jpg” data-large-file=”https://unclinic.ru/wp-content/uploads/2021/09/nuzhno-li-nosit-masku.jpg” loading=”lazy” src=”https://unclinic.ru/wp-content/uploads/2021/09/nuzhno-li-nosit-masku-900×600.jpg” alt=”Нужно ли носить маску” width=”900″ height=”600″ srcset=”https://unclinic.ru/wp-content/uploads/2021/09/nuzhno-li-nosit-masku.jpg 900w, https://unclinic.ru/wp-content/uploads/2021/09/nuzhno-li-nosit-masku-768×512.jpg 768w” sizes=”(max-width: 900px) 100vw, 900px” title=”Антитела IgG и IgM и клеточный иммунитет к COVID-19″>
Антитела IgG сохраняются в организме дольше, чем антитела IgM, и являются основой для защиты от воздействия новой инфекции. При наличии антител IgG и отсутствии антител класса IgM можно с большой вероятностью предположить, что у пациента уже была инфекция COVID-19.
Как работают антитела класса IgM?
Наличие высокого титра антител класса IgM к COVID-19 свидетельствует о том, что в организме есть или недавно была инфекция.
В случае COVID-19 антитела класса IgM и класса IgG обычно появлялись в сыворотке одновременно, уже на ранней стадии заражения, и ровно через 2-3 недели с момента контакта с вирусом. Стоит отметить, что руководящие принципы не рекомендуют определять только антитела класса IgM.
Как проверить антитела к SARS-CoV-2?
Определить количественно антитела к вирусу SARS-CoV-2, можно сдав на анализ образец венозной крови. Количественное определение говорит о точном уровне антител в крови. При желании определить антитела после болезни или прививки, лучше всего делать это не ранее, чем через 2-3 недели после заболевания или второй дозы вакцины. Предварительное определение может еще не обнаружить искомые антитела.
Определение антител не позволяет сделать вывод о текущей инфекции вирусом SARS-CoV-2. Поэтому анализ не следует делать при наличии симптомов COVID-19. Для подтверждения инфекции необходимо обнаружить генетический материал вируса в мазке из носа или горла больного.
С другой стороны, определение антител может быть вспомогательным методом, например, для определения того, можно ли считать тревожные симптомы осложнениями болезни COVID-19.
Что такое клеточный иммунитет?
Клеточный иммунитет, как и гуморальный иммунитет (то есть зависимый от антител) – специфический иммунитет, направленный против специфического антигена. Специфический иммунный ответ возникает в результате контакта с этим антигеном. К вирусу SARS-CoV-2 – это белок S.
В отличие от специфического иммунного ответа, неспецифический иммунитет защищает организм сразу от нескольких различных антигенов.
Клеточный иммунитет зависит от Т-лимфоцитов (один из видов лейкоцитов). Т-клетки неоднородная группа клеток, делящаяся на:
- Цитотоксические лимфоциты. Эти лимфоциты отвечают за разрушение клеток, инфицированных чужеродным антигеном путем апоптоза – запрограммированная гибель клеток;
- Вспомогательные лимфоциты. Способны вырабатывать специальные интерлейкины, дающие возможность другим клеткам иммунной системы, в том числе цитотоксическим лимфоцитам, начать борьбу с антигеном.
COVID-19 и клетки иммунной памяти
После COVID-19 и после вакцинации в организме образуются клетки памяти, относящиеся к В- и Т-лимфоцитам. Благодаря этой информации после повторного контакта с возбудителем организм сможет за короткое время вырабатывать защитные антитела против вируса, что значительно улучшает иммунный ответ организма и дает шанс на более эффективную борьбу с инфекцией.
В свою очередь, клетки памяти, принадлежащие Т-лимфоцитам, после повторного контакта с вирусом смогут быстрее его нейтрализовать и уничтожить уже инфицированные клетки, что ограничивает распространение вируса в организме.
Можно ли не иметь антител, а иметь клеточный иммунитет?
Отсутствие антител, направленных против SARS-CoV-2, не означает, что в организме не выработается какой-либо иммунитет. Антитела – элемент гуморального иммунитета, но есть ещё и клеточный иммунитет, и его нельзя недооценивать.
Следует отметить, что до сих пор неизвестно, как долго антитела сохраняются в крови, однако некоторые научные отчеты показывают, что они обнаруживаются даже через 5 месяцев после начала заболевания.
Наличие антител не обеспечивает 100% защиты от повторного заболевания, но, безусловно, значительно снижает его вероятность. Поэтому, несмотря на наличие антител, необходимо следовать действующим эпидемиологическим рекомендациям.
Нужно ли пациентам, у которых не выработались антитела, вакцинироваться 3-й дозой вакцины от COVID-19?
Обязательных рекомендаций по использованию третьей дозы вакцины от COVID-19 пока нет. Так как вакцина от COVID-19 или болезнь также оставляет клеточный иммунитет, антитела не рассматриваются как фактор, четко определяющий наличие или отсутствие иммунитета. Но новые данные об иммунных механизмах, связанных с COVID-19, исключают такой сценарий в будущем.
Похожее
Вы должны авторизоваться чтобы опубликовать комментарий.
Клеточный иммунитет — теория, основоположники и роль
Тело человека подвержено влиянию множества вредных факторов. Оно защищается от них как может. Теория клеточного иммунитета — это учение, которое обобщенно опытными исследованиями. Его основу составляют механизмы и принципы деятельности иммунной защиты в организме человека. Первые успешные попытки разобраться в иммунной системе сделали двое ученых: русский биолог Илья Мечников и немецкий химик Пауль Эрлих.

Многообразие теорий иммунитета
В ходе эволюции иммунной системы человека развился мощный защитный механизм против бактерий, вирусов и паразитов. Он называется врожденный иммунитет.
Функции врожденного иммунитета осуществляются следующим образом:
- Посредством механической защищенности в процессе вторжения патогенов.
- За счет клеточного иммунитета.
- За счет гуморальных факторов.
Мечников является основоположником клеточной (фагоцитарной) теории иммунитета, а Эрлих смог обосновать гуморальную теорию иммунитета.

Фундаментом гуморального иммунитета служит принцип ликвидации инородных элементов через жидкости внутренней сферы (через кровь). Отличительной чертой процесса является формирование иммунной памяти, препятствующей вторжению в будущем бактерий и вирусов.
Кроме клеточного и гуморального, были и другие теории иммунитета:
- вирусолог М. Ф. Бёрнет разработал клонально — селективную теорию функционирования иммунной защиты;
- Фридрих Брейнль и Феликс Гауровиц выступили инициаторами создания инструктивной теории иммунитета.
- М. Гейдельбергом и Л. Полингом выдвинута новая теория иммунитета, предусматривающая образование комплекса антигенов и антител в виде решетки.
- шведский иммунолог Н. К. Йерне предложил теорию естественного отбора в антителообразовании.
Все эти иммунные теории легли в основу иммунологии как науки, позволили ученым обобщить исторически сложившийся опыт относительно деятельности иммунной системы человека.
Эксперименты Эрлиха с токсинами и антитоксинами
В 1889 году Эрлих на несколько месяцев поехал в Египет лечиться от туберкулеза. Вернувшись в Берлин, он решил оставить прежнюю работу в благотворительной больнице. Вместо этого он продолжил исследование в съемной квартире, которую превратил в частную лабораторию. Эрлих анализировал образцы тканей.
В этой области он уже сделал себе имя. Целью его деятельности было узнать больше о том, что происходит внутри клетки, в частности, как влияют на неё инфекционные болезни. Окрашивая образцы, Эрлих делал видимыми разные участки клетки.
Это также помогало понять химическую природу разных компонентов клетки.

Но опыты требовали много труда и времени. В том же году Эрлих понял, что его опыты с окрашенными тканями ведут его к цели кружным путем.
Он решил испробовать другой подход. Экспериментируя с мышами, Эрлих изучил действие токсинов, выделяемых бактериями. В качестве образца он использовал фитотоксины: белки рицин и абрин. Эрлих ввёл токсины в корм мышей.
Опыт помог открыть и доказать, что если вводить токсины медленно и постепенно, мышь может выдержать во много раз больше, чем смертельная доза. Другими словами, у мышей развивались защитные силы.
Они стали устойчивыми к токсическим веществам, которые нейтрализовались антитоксинами. Теперь Эрлих хотел узнать, взаимодействуют ли токсины и антитоксины напрямую, как при химической реакции или же нужна какая-то третья сила.
С помощью экспериментов Эрлих показал, что токсин и соответствующий антитоксин, полученные из сыворотки крови иммунизированных животных, реагируют друг с другом без участия живых клеток. Токсин и антитоксин соединяются, как любые молекулы при химической реакции.

Эрлих продолжил развивать свои идеи и в 1897 году опубликовал богато иллюстрированную теорию боковых цепей. Он обнаружил, что боковые цепи — это антитоксины, расположенные в клеточных мембранах в определенной форме. Когда токсин связывается с соответствующей боковой цепью, он стимулирует клетку образовывать другие подобные цепи.
Они связывают другие молекулы токсина. Излишек боковых цепей выпускается в кровь, нейтрализуя токсин в плазме даже вне тела, в пробирке.
Победа над дифтеритом и учение Мечникова
Одной из нерешенных медицинских проблем того времени было лекарство от дифтерита. От этой бактериальной инфекции гортани только в одной Германии ежегодно умирали десятки тысяч людей, в том числе дети.
В то время другой великий ученый работал над тем, чтобы создать сыворотку против дифтерита — Роберт Кох. Он нанял Эрлиха, который благодаря своей работе с фитотоксинами мог взять на себя контроль над сыворотками крови и проверку их эффективности.

Эрлих улучшил способы увеличения иммунизирующего эффекта животной крови с антителами. Вместе с Эмилем Адольфом фон Берингом, создателем противодифтерийной сыворотки, Пауль Эрлих добился успеха в получении и промышленном производстве этой сыворотки. Это обеспечило сохранение множества жизней.
Однако многие инфекционные болезни не поддавались лечению сывороткой. Эрлих понял, что у сывороток есть свои ограничения. Он начал проверять влияние химических веществ на инфекции.
Его величайшим успехом в этой новой области стал сальварсан — первое эффективное лекарство от сифилиса. Благодаря этому достижению Пауль Эрлих считается основоположником химиотерапии.
Однако в 1908 году он получил Нобелевскую премию за работу не в области химии, а иммунологии. Эрлих разделил премию с биологом из России Ильей Мечниковым.

По теории Мечникова, возбудители болезни идентифицируются фагоцитами, которые атакуют и уничтожают их. Основу его фагоцитарной теории составили три основных свойства фагоцитов:
- способность фагоцитов защищать и очищать организм от инфекций, токсинов и продуктов распада тканей;
- возможность фагоцитов секретировать биологически активные вещества и ферменты;
- способность фагоцитов представлять (располагать) антигены на мембране клетки.
В мае 1882 года из-за политических интриг Мечников вынужден был покинуть Одесский университет. Оскорблённый, он уехал с семьей в Италию, чтобы спокойно продолжать научную работу.
В Мессине Мечников занялся биологическим развитием низших морских животных. Во время опытов он скармливал морским звездам красящие вещества. Мечников заметил, что частички краски окружают и поглощают некоторые клетки. Он понял, что эта часть защитной системы против захватчиков.
Роль фагоцитов в борьбе с болезнями
Мечников поставил в Мессине свой решающий эксперимент. Он надеялся, что полупрозрачные личинки морских звезд позволят наблюдать за процессом, который он хотел изучить. В саду он нашел инородное тело, довольно мелкое для его опыта. Он решил использовать острые шипы розы, чтобы ввести их личинкам.
С помощью вазелина Мечников подготовил предметное стекло, чтобы капнуть на него каплю морской воды с личинками. Затем началась самая сложная работа под микроскопом. Мечников осторожно вел розовый шип в личинку. За ночь фагоциты окружили шип, чтобы сразиться с пришельцем.
На основе этого опыта Мечников развил теорию фагоцитов. Основатель фагоцитарной теории иммунитета работал над ней 25 лет. Среди прочего Мечников наблюдал активную роль фагоцитов в борьбе с патогенами на примере водяных блох. Часто их инфицирует грибки-паразиты, и в результате блохи умирают.

Мечников заметил, что иногда вскоре после заражения, споры грибка уничтожаются фагоцитами, и блоха выживает. Он наблюдал, как фагоциты успешно борются с инфекционной болезнью.
Позже в экспериментах с теплокровными, он также заметил, что прививка от болезни, например, сибирской язвы, усиливает активность фагоцитов. Мечников сделал вывод, что суть иммунитета — это обучение фагоцитов бороться с конкретным патогеном.
Большинство его ученых-коллег сочли теорию фагоцитов настолько невразумительной, что отвергли её, даже не пытаясь опровергнуть опытами. Даже Роберт Кох отверг гипотезу Мечникова, но 20 лет спустя он признал, что был неправ.
Ученые разделились на два лагеря: одни были за теорию боковых цепей Эрлиха, другие — за фагоциты Мечникова. Казалось невозможным, чтобы существовали и фагоциты, и антитоксины. Только после 1900 года было найдено связующее звено для двух теорий. И нашел его не кто иной, как Мечников.
Взаимодействие антител и антигенов
В 1903 году теория опсонинов Алмрота Райта (1861−1947) внесла большой вклад в развитие учения. По теории Райта, кровь содержит вещества опсонины, которые делают атакующие клетки, уязвимыми для фагоцитов. Современной науке известно химическое строение антител, их теперь называют антитоксины или опсонины.

Более тысячи аминокислот образуют сложную молекулу, напоминающую по форме букву Y. Такова базовая структура всех антител. Но места связывания на конце двух рожек (Y), позволяют составлять миллионы вариаций. Такое связывание позволяет каждому антителу подходить к конкретному антигену. Это может быть инородный токсин, бактерия или вирус.
На поверхности каждого антигена есть формы, к которым могут прикрепиться лишь конкретные антитела. Только если антитело подходит к антигену как ключ к замку, захватчика можно нейтрализовать. Молекулы антител слипаются с антигенами, которых теперь могут уничтожить фагоциты.
Антитела и фагоциты работают вместе, но не фагоциты решают, атаковать ли чужеродную клетку. Патрулируя по организму, фагоциты предоставляют лимфоцитам — клеткам-помощникам, собственный материал — тело, а лимфоциты решают нужно ли принимать защитные меры.

Если нужно, они дают команду фагоцитам начать специфическую атаку. Сегодня науке известны главные компоненты иммунной системы и их функции. Иммунология давно стала отдельной отраслью медицины.
В ней кроется ключ ко многим нерешенным медицинским проблемам. От многих болезней существуют вакцины, но человечество по-прежнему бессильно против СПИДа. Это болезнь, чей патоген ВИЧ атакует клетки человеческой иммунной системы.
Сегодня современные генетические методы помогают определить слабые места вируса, которые можно атаковать с помощью лекарств. В будущем иммунологи смогут обеспечивать людей новыми формами лечения рака, аутоиммунных болезней и ослабленного иммунитета, революционными терапиями, которые по масштабу и эффективности будут сравнимы с открытием пенициллина.
4. 13. 091 Фагоцитарная теория иммунитета Мечников
4.13 Физиология, медицина
4.13.091 Фагоцитарная теория иммунитета Мечникова
Зоолог, эмбриолог, физиолог, бактериолог, иммунолог, патолог; лектор, пропагандист; создатель первой русской школы микробиологов, иммунологов и патологов; профессор Новороссийского университета; почетный доктор Кембриджского университета; почетный член Петербургской АН, член Французской академии медицины, Шведского медицинского общества и других зарубежных АН, научных обществ и институтов; организатор и руководитель первой в России Одесской бактериологической станции для борьбы с инфекционными заболеваниями; создатель и заведующий лабораторией в Пастеровском институте (Париж), заместитель директора этого института; лауреат премии К. Бэра (вместе с А.О. Ковалевским), Нобелевской премии по физиологии и медицине (совместно с П. Эрлихом); обладатель медали Копли Лондонского королевского общества и других наград и знаков отличия — Илья Ильич Мечников (1845—1916) является одним из основоположников эволюционной эмбриологии, творцом сравнительной патологии воспаления, первооткрывателем фагоцитоза и внутриклеточного пищеварения, родоначальником научной геронтологии.
Выдающимся достижением биолога стала его фагоцитарная теория иммунитета.
Убежденный и не раз наученный горьким опытом, что «в России на кафедрах хорошие чиновники предпочтительнее самых выдающихся ученых», И.И. Мечников своей научно-педагогической деятельностью занимался большей частью за пределами нашей страны в добровольном изгнании в Италии, Германии, Франции.
Тем не менее все свои труды Илья Ильич посвятил России, печатал их на русском языке в российских изданиях, поддерживал постоянную связь с русскими учеными, основал первую русскую научную школу микробиологов, иммунологов и патологов, из стен которой вышло немало выдающихся исследователей.
Многогранная деятельность ученого затрагивала самые разные области биологии и медицины, но наиболее впечатляющих научных результатов Мечников добился в эмбриологии и геронтологии, а также в иммунологии и примыкающей к ней патологии. Вкратце скажем о первых двух и подробнее остановимся на трудах биолога по иммунитету.
За исследования по эмбриологии беспозвоночных (головоногих моллюсков, насекомых, ресничных червей — планарий) подчиненные сверхзадаче — доказательству эволюции, Мечников вместе с зоологом А.О. Ковалевским получил престижную премию К. Бэра.
Ученые установили единство развития позвоночных и беспозвоночных животных и заложили основы новой отрасли биологии — эволюционной эмбриологии.
Мечников выдвинул также теорию «паренхимеллы» (фагоцителлы) — вымершего предка многоклеточных животных, сыгравшую большую роль в развитии эволюционного учения.
Выясняя вопросы старения человека, Мечников установил несколько причин, влияющих на преждевременную старость и смерть. Прежде всего — это самоотравление организма микробными и прочими ядами. Для оздоровления кишечной флоры биолог предложил целый ряд проверенных, в т.ч. и на себе, мер: стерилизацию пищи, кисломолочные продукты (болгарский йогурт — простокваша, заквашенная с помощью болгарской палочки, кавказский кефир), живую культуру микроорганизмов — пробиотики, ограничение потребления мяса и т.п.
Мечников полагал, что жизнь человека должна быть долгой и счастливой и завершаться «спокойной естественной смертью». Для этого нужно одно умение — «жить правильно». Это состояние ученый нарек ортобиозом. («Этюды о природе человека», 1903; «Этюды оптимизма», 1907).
Для большинства людей это учение скорее утопия, но для его приверженцев — панацея от многих болезней и досрочного увядания.
Путь Мечникова к фагоцитарной теории иммунитета был долгий и трудный. К тому же он сопровождался непрерывными войнами с противниками этого подхода.
Начался он в Мессине (Италия), где ученый наблюдал за личинками морской звезды и морскими блохами. Патолог заметил, как блуждающие клетки (названные им фагоцитами — пожирателями клеток) этих созданий окружают и поглощают чужеродные тела, а заодно резорбируют (рассасывают) и уничтожают другие ткани, не нужные более организму.
К идее фагоцитов Мечников пришел ранее при изучении внутриклеточного пищеварения в подвижных клетках соединительной ткани беспозвоночных (амеб, губок, и др.), когда клетки захватывают твердые пищевые частицы, и постепенно их переваривают. У высших животных типичными фагоцитами являются белые клетки крови — лейкоциты.
В этой борьбе между фагоцитами организма и поступившими извне микробами и в сопровождающем эту борьбу воспалением Мечников усмотрел суть любой болезни, ее философию, если угодно.
Эксперименты биолога были гениальными в своей простоте. Искусственно вводя в тело личинки инородные тела (например, шип розы), ученый демонстрировал их захват, изоляцию или уничтожение фагоцитами. Достаточно прозрачные (как морская звезда) доводы русского ученого хоть и взбудоражили научную общественность, но и настроили ее против данной трактовки заболевания организма.
Дело в том, что многие биологи (особенно немецкие — Р. Кох, Г. Бухнер, Э. Беринг, Р. Пфейфер) были поборниками возникшей в то же время т.н. гуморальной теории иммунитета, согласно которой чужеродные тела уничтожаются не лейкоцитами, а другими веществами крови — антителами и антитоксинами. Как оказалось, этот подход правомерен и согласуется с фагоцитарной теорией.
Исследуя фагоциты десятки лет, Мечников заодно изучал холеру, тиф, сифилис, чуму, туберкулез, столбняк, другие заразные заболевания и их возбудителей. Именно изучение иммунитета при инфекционных заболеваниях человека и животных — от простейших до высших позвоночных, с позиций клеточной физиологии, специалисты отнесли к главной заслуге русского ученого.
Тем более что результаты его исследований стали фундаментом новой отрасли биологии и медицины — сравнительной патологии, а решенные школой Мечникова вопросы бактериологии и эпидемиологии стали основой современных методов борьбы с инфекционными заболеваниями.
Первый доклад из серии многочисленных работ, посвященных фагоцитарной (целлюлярной) теории — «О целебных силах организма» Мечников сделал на 7-м съезде русских естествоиспытателей и врачей в Одессе в 1883 г.
В своих «Лекциях по сравнительной патологии воспаления» (1892) биолог обосновал представление о патологических процессах, как о реакциях организма, его «норме».
Итогом многолетних исследований иммунитета стал классический труд Мечникова «Невосприимчивость в инфекционных заболеваниях» (1901). В нешуточной борьбе идей ученому удалось отстоять свою теорию.
«Биология и медицина обязаны И.И. Мечникову… существенными широкими обобщениями, положившими начало ряду наиболее прогрессивных направлений современной биологии и медицины» (http://nplit.ru/). А мы все — потребители научных достижений русского ученого — еще и его раздумьями о жизни, смерти, физическом и нравственном здоровье человека. «Решение задачи человеческой жизни должно неизбежно повести к более точному определению основ нравственности. Последняя должна иметь целью не непосредственное удовольствие, а завершение нормального цикла существования».
P.S. В 1908 г. И.И. Мечникову была вручена Нобелевская премия по физиологии и медицине «за труды по иммунитету». В приветственной речи говорилось о том, что «Мечников положил начало современным исследованиям по. иммунологии и оказал глубокое влияние на весь ход ее развития».
Поскольку к тому времени ученый уже более 20 лет жил во Франции и работал в Пастеровском институте, Нобелевский комитет сделал официальный запрос — является ли будущий нобелиат русским или французом. «Илья Ильич с гордостью ответил, что он всегда был и продолжает быть русским» (Д.Ф. Острянин).
Фагоцитарная теория иммунитета
Сейчас определение «иммунитет» звучит так часто, что с его значением знаком каждый школьник. Сложно поверить, что всего сто с небольшим лет назад об иммунной системе не имели понятия даже выдающиеся умы своего времени.
Впрочем, подозревать о наличии у организма особой защиты люди начали еще очень давно. В Древнем Китае лекари делали «инъекции» из содержимого оспенных пузырьков здоровым людям, чтобы предохранить их от заболевания. Позже кровь людей, переболевших инфекционными болезнями, стали переливать тем, кого пытались защитить от этих болезней. Но все это были «кустарные» эксперименты. К пониманию сути иммунных процессов ученые приблизились много позже…
От Пастера к Мечникову
Известный врач Луи Пастер считал, что невосприимчивость организма к болезням определяется тем, что тело человека не подходит микробам как питательная среда. Но у этой теории было слишком много слабых мест, так что ученый и сам не настаивал на ее абсолютной правильности. Другие врачи выдвигали свои предположения, но они также были далеки от истины.
В конце XIX века русский биолог И.И.Мечников выдвинул свою  гипотезу на этот счет. Наблюдая за примитивными организмами, изучая кровь и ткани животных и человека, он нашел во всех этих материалах общие черты. В них присутствовали особые амебообразные подвижные клетки, которые захватывали пищевые или другие инородные твердые частицы (в том числе и патогены), и переваривали их.
гипотезу на этот счет. Наблюдая за примитивными организмами, изучая кровь и ткани животных и человека, он нашел во всех этих материалах общие черты. В них присутствовали особые амебообразные подвижные клетки, которые захватывали пищевые или другие инородные твердые частицы (в том числе и патогены), и переваривали их.
Эти клетки он назвал фагоцитами, что в буквальном переводе означает «пожиратели». Открытие фагоцитоза продолжилось углубленным исследованием этого явления. На основе дальнейшего изучения иммунитета, которое заняло у Мечникова более 20 лет, он выдвинул свою знаменитую фагоцитарную теорию.
Фагоцит захватывает бактерии
Основы фагоцитарной теории:
Учение о фагоцитозе может быть вкратце представлено следующими тезисами.
• Фагоцитоз – это процесс захвата и переваривания особыми клетками крови и тканей различных частиц: бактерий, вирусов, компонентов инородных тел, остатков разрушенных тканей, погибших клеток и т.д.
• Иммунный фагоцитоз осуществляется клетками-фагоцитами. К ним относятся несколько разновидностей, главным образом это те или иные формы лейкоцитов. Сам Мечников делил все фагоциты на микрофаги и макрофаги, но сейчас это разделение выглядит устаревшим. Современное учение о фагоцитозе гласит, что фагоциты следует разделять на профессиональные, которые направленно борются с конкретными объектами, и не профессиональные, работающие менее эффективно. Впрочем, не будем развивать эту тему далее, потому что она не имеет прямого отношения к теории Мечникова.
 • Последовательность процессов при фагоцитозе включает несколько стадий. Во время первой из них «радары» фагоцитов засекают присутствие в организме вредоносного объекта, а на последней фагоцит избавляется от остатков захваченной и переваренной частицы.
• Последовательность процессов при фагоцитозе включает несколько стадий. Во время первой из них «радары» фагоцитов засекают присутствие в организме вредоносного объекта, а на последней фагоцит избавляется от остатков захваченной и переваренной частицы.
• Фагоцитоз – это процесс, в результате которого фагоцит не просто уничтожает «интервента» безо всякого следа. Он выставляет на поверхность своей мембраны добытый «трофей» – антигены переваренной частицы. После этого, вступая в контакт с другими клетками иммунитета (лимфоцитами и др.), фагоцит передает им информацию о вредоносном объекте, чтобы те сохраняли повышенную бдительность и при встрече с вредоносным объектом были готовы его уничтожить.
Лимфоцит
От Мечникова к Лоуренсу
После того как И.И.Мечников получил за свою теорию Нобелевскую премию, его многочисленные ученые-последователи существенно расширили знания о том, что представляет собой иммунный фагоцитоз и как он происходит. Была определена конкретная последовательность процессов при фагоцитозе, пополнена копилка знаний о других сторонах иммунной защиты (в частности, обнаружен гуморальный иммунитет). В результате открытие фагоцитоза Мечниковым закономерно привело к новому научному прорыву – выделению Генри Лоуренсом особого вещества: фактора переноса.
Фактор переноса, или трансфер фактор, представляет собой  пептид, образующийся лимфоцитами. Он содержит в себе накопленную этими клетками информацию, которую они получили на протяжении своей жизни: в процессе непосредственной встречи с патогенами, а также в результате фагоцитоза (в этом случае им ее передали клетки-фагоциты).
пептид, образующийся лимфоцитами. Он содержит в себе накопленную этими клетками информацию, которую они получили на протяжении своей жизни: в процессе непосредственной встречи с патогенами, а также в результате фагоцитоза (в этом случае им ее передали клетки-фагоциты).
Явление фагоцитоза и процесс образования информационных пептидов тесно связаны. По этой причине современный препарат Трансфер Фактор как нельзя лучше подходит для укрепления фагоцитарного звена иммунитета. Созданный на основе природного фактора переноса, он эффективно влияет на активность фагоцитов, повышает их «бдительность» по отношению к заболеваниям и укрепляет иммунную систему в целом.
Чтобы иммунитет был по-настоящему неуязвим, человеку больше не нужно лично и тесно «знакомиться» с инфекциями, токсинами и другими вредными объектами. Достаточно регулярно принимать Трансфер Фактор и просто беречь свое здоровье…
